Las propiedades más especiales de los compuestos ionicos son:
- Altos puntos de fusión.
- Conductividad de la corriente eléctrica y el calor
- Solubilidad en agua
Pero de igual forma, no podemos generalizar a todos los compuestos en las categorías anteriores ya que estas propiedades dependerán del sistema que se esta estudiando.
Factores que alteran las propiedades de los compuestos ionicos:
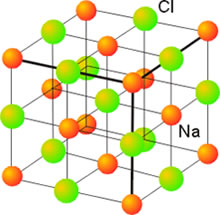
Como ya sabemos, los compuestos ionicos se pueden representar como una red de puntos fijos donde los aniones y los cationes ejercen y reciben atracciones multinacionales, debido a que las celdas que forman la red se distribuyen en tres dimensiones y permiten que los vecinos laterales, los vecinos superiores e inferiores y por consiguiente los vecinos que están de frente o atrás de un átomo interaccionen y formen enlaces químicos por medio de fuerzas electrostáticas generadas a partir de las cargas contrarias que poseen los iones. Esta característica de enlace produce que los compuestos ionicos no se puedan moldear tan fácilmente como los metales.
Mediante este modelo podemos deducir la existencia de interacciones fuertes por parte de los iones y la estabilidad de estas.
Para continuar debemos conocer el concepto de "Energía reticular" la cual se define como:
La conductividad eléctrica y calorífica depende de su solubilidad en agua, ya que para que conduzca la electricidad los átomos tienen que estar ionizados y libres por el medio o también la especie química debe estar fundida.
Para continuar debemos conocer el concepto de "Energía reticular" la cual se define como:
Cantidad de energía requerida para separar completamente un mol de un compuesto iónico en sus iones gaseosos. (También llamada energía de red).
Esta energía de red, puede ser muy alta o muy baja, dependiendo de qué tan fuerte sea la interacción por parte de los iones en el cristal.
Los factores que afectan a la energía reticular son:
- Tamaño de los iones
- Carga de los iones
A mayor tamaño de los iones, observaremos que hay menor área de contacto y por lo tanto las interacciones son menores a comparación de la que generan los iones muy pequeños, por lo que la energía reticular disminuye al descender la fuerza de las interacciones
El otro factor muy importante son las cargas de los iones, a mayor concentración de las cargas, mayor y más fuertes interacciones por parte de los iones, por lo que la energía reticular aumenta.
Si la energía reticular es muy grande para un compuesto quiere decir que al momento de intentar solubilizar, la energía de hidratación (del agua) no podrá superar a la de la red y por lógica el compuesto será INSOLUBLE y a su vez, como la red se mantiene unida fuertemente necesitará más calor para poder romper las interacciones y esta cuestión de calor se verá reflejada en el punto de fusión y la dureza del compuesto.


No hay comentarios:
Publicar un comentario